Puntea musculară coronariană
Autor:
Dr. Nicolae Cârstea
Dr. Mereuţă Adrian
IUBCV „CC Iliescu” Bucureşti
Arterele coronare au traiectul, în mod normal, pe suprafaţa epicardică a miocardului.
Puntea musculară (PM) este o anomalie congenitală în care un segment al arterei coronare prezintă un traseu intramuscular sub o „punte” de miocard.(vezi figura) Acest traseu cauzează compresia sistolică a vasului, lucru care determină modificări hemodinamice care pot fi asociate cu angină, ischemie miocardică, sindroame coronariene acute, disfuncţie sistolică ventriculară stângă, aritmii și moarte subită.
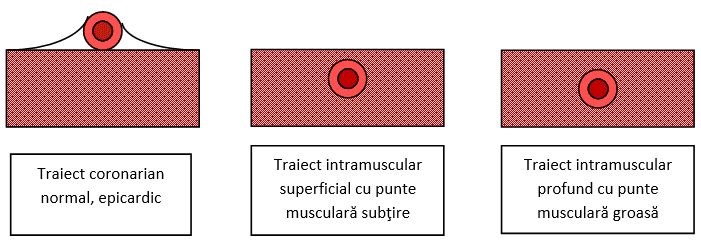 Artera coronară poziţionată epicardic, în mod normal şi intramuscular, în cazul punţii musculare. Consecinţele acestei anomalii depind de profunzimea la care se află artera în interiorul miocardului şi de lungimea porţiunii tunelizate. (după 1)
Artera coronară poziţionată epicardic, în mod normal şi intramuscular, în cazul punţii musculare. Consecinţele acestei anomalii depind de profunzimea la care se află artera în interiorul miocardului şi de lungimea porţiunii tunelizate. (după 1)
Prevalenţa punţii musculară este raportată foarte diferit în funcţie de metoda diagnostică folosită şi de grupul de pacienţi la care este aplicată. Astfel, după coronarografie, metoda clasică de diagnostic, prevalenţa este de 0,5-2,5%, pe când autopsia dă o prevalenţă mult mai mare, de 15-85% (în medie 25%).2,3 Angiografia prin tomografie computerizată dă cifre asemănătoare autopsiei. Probabil ca aceste ultime metode contablizează toate cazurile, pe când coronarografia vizualizează doar pe cele semnificative hemodinamic. La anumite categorii de pacienţi, puntea musculară este deosebit de frecventă: până la 80% la pacienţii cu cardiomiopatie hipertrofică şi 33% la pacienţii cu transplant cardiac.2
Puntea musculară afectează cel mai frecvent artera descendentă anterioară (ADA) în segmentul mijlociu, însă anatomic, dar nu şi angiografic, s-a descris interesarea arterei circumflexe (ACX), coronarei drepte (ACD) sau a ramurilor diagonale şi marginale.4 Anatomia punţii musculare este foarte variată, putând avea o grosime care variază de la 1 la 3,8 mm şi o lungime de la 2,3 la 42,8 mm.5 Cu cât traiectul intramuscular e mai profund şi mai lung, cu atât consecinţele hemodinamice sunt mai importante.(vezi figura)
Fiziopatologia punţii musculare este substanțial diferită față de cea a stenozelor fixe. Deoarece obstacolul este doar sistolic, iar fluxul coronarian este predominant în diastolă (în proporţie de 85% la nivelul ADA, respectiv 55% în ACD), impactul asupra vascularizării coronariene ar trebui să fie redus.6 Totuşi, studiile imagistice intracoronariene au demonstrat ca aria luminală este afectată și în timpul diastolei precoce, cât şi a celei medii afectând deci fluxul coronarian diastolic.3 Modificările hemodinamice datorate punţii musculare favorizează apariţia aterosclerozei în porţiunea imediat proximală punţii. În schimb, porţiunea tunelizată intramiocardic nu este obişnuit afectată de ateroscleroză, probabil datorită modificărilor structurale ale peretelui arterial: subţierea intimei care conţine predominat fibre musculare de tip “contractil”, ce nu se asociază cu ateroscleroza.7
Puntea musculară poate produce ischemie sau disfuncţie reversibilă de ventricul stâng (VS) mai ales în condiţii de tahicardie prin scurtarea diastolei. Sindromul coronarian acut şi moartea subită pot fi datorate complicaţiilor trombotice produse prin lezarea intimei în zona intramusculară sau de complicaţiile plăcii aterosclerotice din porţiunea proximală.5 Alte mecanisme implicate ar putea fi spasmul coronarian în porţiunea tunelizată sau fibroza miocardului ce formează puntea musculară.8
Diagnosticul PM se face, în mod clasic, angiografic prin vizualizarea reducerii sistolice a diametrului coronarei la care se adaugă şi un aspect de “mulgere”, atunci când reducerea sistolică a vasului este > 70%. Evidenţierea compresiei sistolice poate fi accentuată de administrarea de nitroglicerină care dilată restul vasului. Doppler-ul intracoronarian prezintă un aspect caracteristic de „spike and dome” sau de ”vârf de deget” prin creşterea protodiastolică a vitezei fluxului datorată tocmai persistenţei compresiei şi la începutul diastolei. Ecografia intravasculară (IVUS) demonstrază direct compresia sistolică (excentrică sau concentrică) şi permite măsurarea severităţii acesteia. Se recomandă ca măsurarea rezervei de flux (FFR) să se facă după provocare cu dobutamină şi nu cu adenozină. Pentru evaluarea ischemiei, se foloseşte FFR diastolic, deoarece cel global este artefactat de creşterea presiunii sistolice.2 Tomografia computerizată evidenţiază corect incidenţa PM, însă informaţiile sunt doar anatomice şi nu funcţionale.
Puntea musculară este considerată în general o condiţie benignă, însă este asociată uneori cu angină, spasm coronarian, ischemie miocardică, infarct miocardic acut, disfuncţie de VS, aritmii sau moarte subită. Aceste evenimente sunt foarte rare la pacienţii cu PM, iar relaţia de cauzalitate nu este clară. Totuşi testele de provocare au indus ischemia în 21-88% din cazuri.9 Severitatea ischemiei a fost determinată în primul rând de gradul compresiei sistolice şi mai puţin de lungimea sau localizarea PM.
Tratamentul punţii musculare simptomatice este în primul rând medicamentos. Pacienţii asimptomatici nu necesită tratament. Pentru pacienţii simptomatici, betablocantele şi blocantele de calciu non-dihidropiridinice reprezintă tratamentul de elecţie, iar nitraţii sunt contraindicaţi. Pentru rarele cazuri, în care tratamentul medicamentos nu controlează simptomatologia sau în caz de complicaţii asociate cu puntea musculară, se indică tratamentul radical al bolii, intervenţional sau chirurgical.
Stentarea coronariană a dus la ameliorarea simptomatologiei, însă e complicată uneori de fracturi ale stentului sau perforaţie a coronarei şi are o rată mare de restenoză (24 – 50%) chiar cu utilizarea stenturilor active.2,10 În privinţa tratamentului leziunilor aterosclerotice proximale de PM, un studiu pe 70 de pacienţi a arătat că acoperirea cu stentul şi a porţiunii intramiocardice a dus la creşterea necesarului de reintervenţie (pentru restenoză) la 24% faţă de 3% la cei la care plasarea stentului s-a oprit înainte de PM.11
Există două abordări chirurgicale în PM: rezecţia fibrelor musculare (miotomie chirurgicală) ce acoperă artera sau bypass efectuat după porţiunea intramiocardică, ambele cu ameliorare spectaculoasă a simptomatologiei. Miotomia este procedura de elecţie, bypass-ul fiind rezervat cazurilor cu traseu intramiocardic profund, în care miotomia se poate complica cu perforaţie ventriculară sau favoriza dezvoltarea anevrismelor. Deşi există un risc pentru bypass datorat fluxului competitiv, urmărirea la 3 ani nu a evidenţiat ocluzia grafturilor.2
În concluzie, puntea musculară este o anomalie congenitală frecventă (25% din populaţie), cu prognostic benign în marea majoritate a cazurilor. Rareori este simptomatică prin angină sau este asociată cu infarct miocardic sau aritmii. În aceste cazuri, tratamentul de elecţie este medicamentos, cu betablocant sau blocanţi de calciu non-dihidropiridinici. În cazurile severe sau refractare, se poate efectua intervenţie chirurgicală de rezecţie a punţii musculare. Bypass-ul aortocoronarian şi stentarea reprezintă alternative posibile la miomectomie.
Bibliografie:
1. Tarantini G, Migliore F, Cademartiri F, Fraccaro C, Iliceto S. Left anterior descending artery myocardial bridging: a clinical approach. J Am Coll Cardiol 2016 Dec 27; 68(25): 2887-2899.
2. Lee MS, Chen CH. Myocardial bridging: an up-to-date review. J Invasive Cardiol 2015; 27(11): 521-528.
3. Bourassa MG, Butnaru A, Lesperance J, Tardif JC. Symptomatic myocardial bridges: overview of ischemic mechanisms and current diagnostic and treatment strategies. J Am Coll Cardiol 2003; 41: 351-359.
4. Mohlenkamp S, Hort W, Ge J, Erbel R. Update on myocardial bridging. Circulation 2002; 106: 2616-2622.
5. Yuan SM. Myocardial bridging. Braz J Cardiovasc Surg 2016; 31: 60-62.
6. Marcus JT, Smeenk HG, Juijer JP, et al. Flow profiles in the left anterior descending and the right coronary artery assessed by MR velocity quantification: effects of through-plane and in-plane motion of the heart. J Comput Assist Tomogr. 1999; 23: 567–576.
7. Risse M, Weiler G. Die koronare Muskelbrücke und ihre Beziehung zu lokaler Koronarsklerose, regionaler Myokardischämie und Koronarspasmus. Eine morphometrische Studie. Z Kardiol. 1985; 74:700–705.
8. Hostiuc S, Curca GC, Dermangiu D, Dermengiu S, Hostiuc M, Rusu MC. Morphological changes associated with hemodynamically significant myocardial bridges in sudden cardiac death. Thorac Cardiovasc Surg 2011; 59(7): 393-8.
9. Tang K, Wang L, Shi R, et al. The role of myocardial perfusion imaging in evaluating patients with myocardial bridging. J Nucl Cardiol. 2011; 18:117–122.
10. Attaran S, Moscarelli M, Athanasiou T, Anderson J. Is coronary artery bypass grafting an acceptable alternative to myotomy for the treatment of myocardial bridging? Interact Cardiovasc Thorac Surg. 2013; 16(3): 347-349.
11. Tsujita K, Maehara A, Mintz GS, et al. Impact of myocardial bridge on clinical outcome after coronary stent placement. Am J Cardiol. 2009; 103:1344–1348.

Puntea musculară este un subiect suficient de controversat și în prezent, atât prin modul de abordare și interpretare a datelor din procedurile de diagnosticare și evaluare, cât și prin modul de abord terapeutic, ținând cont de necesara individualizare a leziunii și de consecințele ei evaluabile nu tocmai direct.
Metoda angiocoronarografică este cea mai trivială, firește, cea mai fiabilă și mai accesibilă pare Angio CT, dar într-o perspectivă strict morfologică. Documentarea ischemiei se poate face nu doar prin procedurile enunțate ci mai ales prin SPECT de efort farmacologic, cu evidențierea masei ischemice (minimum 5% din masa VS), exact ca în cazul leziunilor coronariene provocatoare de ischemie de efort.
Nu este cert faptul că aritmogenitatea leziunii funcționale este aleatoare, ea depinde mai degrabă de proporția de miocard ischemic precizată. Mai mult, studii mai noi contrazic ipoteza endoteliului neatacabil ateromatos din zona tunelului intramiocardic coronarian. Prin urmare, ideea de a stenta strict zona pretunelară este mai degrabă păguboasă, în ciuda aparențelor presionale intermitente, pentru că procedura duce frecvent la disectie neacoperită, la plăci rapid evolutive, chiar la zona de conjuncție, și la tromboze coronariene în aval. Este preferată stentarea completă, firește, identificând-se stenturile cu forța radiară cea mai potrivită, principalul pericol fiind tocmai deformarea extrinsecă a stentului. Rezecția bandeletei musculare pare o procedura facilă, atunci când aceasta nu este amplă, cu pagubă miofibrilară importantă. By-pass-ul coronarian cu mamară internă stângă este discutabil, el depinde tot de severitatea și amploarea ischemiei, de traiectul intramiocardiac al descendentei anterioare, incidența fluxului competitiv fiind, altfel, suficient de mare.
FFR diastolic nu este de un real folos în economia evaluării. Nu este lipsită de sens și evaluarea rezervei coronariane de flux distale, nu doar gradientul FFR. De multe ori, după perioade suficiente disfuncționale, aceasta apare alterată, cu consecințele corespunzătoare. Când FEVS este peste 45%, asocierea betablocanților cu benzotiazepine sau fenilalchilamine și interdicția fermă de nitrați se impun ca primă linie farmacoterapică.
În realitate, o punte musculară simptomatică este o problemă, și nu doar în perspectivă imediată, a simptomelor disconfortante, ci și în cea a miocardului amenințat. Cât despre puntea musculară de pe teritoriul circumflexei, mai degrabă aceasta pune și probleme aritmice, existând statistici în acest sens. Oricum este mult mai rară și mai puțin simptomatică.
Prof. Dr. Lucian Petrescu - IBCV Timișoara
